La entropía es otro de esos conceptos que dejan volar nuestra imaginación.
Principalmente es por esa “oscura” asociación entre entropía y desorden.
Cuando eso del desorden generalmente no queda claro.
Sin embargo, la entropía tiene un significado físico muy profundo a pesar de que no es más que un número.
LO MACRO Y LO MICRO:
Para entender qué es lo que cuantifica la entropía hemos de introducir dos conceptos:
- Macroestado
- Microestado
Hablamos del macroestado de un sistema cuando identificamos dicho sistema por sus características macroscópicas.
Decir esto último no es decir mucho, así que expliquemos lo que son las características macroscópicas.
Hablamos de dichas características a nivel macroscópico a aquellas que no dependen de la constitución más básica del sistema.
Magnitudes como la temperatura, el volumen, la presión, incluso la apariencia que tiene un sistema a nuestros ojos, se consideran características macroscópicas.
Ninguna de ellas depende de que el sistema esté constituido por átomos, por moléculas o por alguna otra cosa.
No depende de las interacciones entre los constituyentes básicos del sistema.
Sin embargo, hablamos de microestado a aquel estado que viene descrito por las propiedades microscópicas del mismo.
Es decir, identificar sus constituyentes, sus posiciones, sus energías, sus interacciones individuales, etc.
Aquí entonces tenemos un juego de niveles.
Un sistema se puede describir microscópicamente (identificando sus constituyentes y sus magnitudes características) o bien se puede describir macroscópicamente (identificando sus propiedades macroscópicas).
Es de “sentido común” (sí, aquí si podemos usarlo) que ambas descripciones han de ser consistentes.
Es decir, dado un microestado uno ha de poder asociarle un macroestado dado.
Pero el punto clave viene de qué pasa cuando nos dan un macroestado.
Si identificamos un macroestado en general tendremos una multitud de microestados compatibles.
Es decir, tendremos muchas configuraciones microscópicas (distintas posiciones de los elementos básicos del sistema, o distintas velocidades, o distintos giros, o distintas energías, etc) que darán justamente el macroestado que tenemos entre manos.
Basta pensar que tenemos un vaso de agua encima de la mesa, sabemos que el agua está compuesta por moléculas y que esas moléculas se mueven, se atraen, se repelen, colisionan, vibran, rotan, etc.
Es decir, a nivel microscópico el sistema está cambiando continuamente, pero a nuestra vista el vaso de agua es el mismo.
Por lo tanto, muchos (muchísimos) microestados dan lugar a un macroestado dado.
¿QUÉ ES LA ENTROPÍA?
Pues simplemente es un número (con determinadas unidades que se introducen para la consistencia de la termodinámica) que no es más que el número de microestados  compatibles con un macroestado dado.
compatibles con un macroestado dado.
Es decir, yo tengo un macroestado (con una temperatura, una energía total fija, etc), ahora me molesto en contar cuantos microestados dan lugar al mismo. Ese número, representado por  nos dará precisamente la entropía del sistema en ese estado.
nos dará precisamente la entropía del sistema en ese estado.
La entropía se calcula a través del logaritmo de dicho número, multiplicado por la constante de Boltzmann 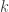 (que es la que introduce las unidades adecuadas)
(que es la que introduce las unidades adecuadas)
Y ESO DEL DESORDEN…
Aquí cuando hablamos del desorden simplemente nos referimos a que hay más configuraciones microscópicas compatibles con un macroestado dado.
Ni más, ni menos.
No es ninguna entelequia, es simplemente que a mayor número de microestados compatibles con un macroestado decimos que hay más desorden.


No hay comentarios:
Publicar un comentario